武汉博欧特生物科技有限公司
入驻年限:11 年
- 联系人:
王定涛
- 所在地区:
湖北 武汉市 洪山区
- 业务范围:
试剂、抗体、ELISA 试剂盒、技术服务、体外诊断
- 经营模式:
代理商
推荐产品
公司新闻/正文
补体末端C5b-9复合物 | 抗肿瘤&肿瘤促进作用
人阅读 发布时间:2023-05-09 10:18

人类体细胞的癌变涉及一系列遗传和表观遗传改变,最终导致恶性组织的产生。
迄今为止,癌细胞有七个关键改变:
- 生长信号的自给自足;
- 对生长抑制剂不敏感;
- 逃避细胞凋亡;
- 实现可复制的永生;
- 持续血管生成;
- 组织侵袭(转移);
- 癌症相关炎症(CRI)的存在。
CRI的基本协调因子是肿瘤相关炎症细胞(巨噬细胞,成纤维细胞,T细胞和髓源性抑制细胞)及其分泌的趋化因子和细胞因子,以及肿瘤微环境中的“补体活化”。
癌细胞与补体系统成分的相互作用非常复杂,导致对癌细胞有利或有害的结果。目前,我们只探究到这些相互作用的“冰山一角”。
补体系统代表了先天免疫的有效武器库,也是先天免疫和适应性免疫之间的接口。“补体系统”是对抗侵入性病原体和有效清除碎片的祖chuan工具,补体系统可能以多种形式影响癌症。
当癌细胞与补体系统相遇时,可以通过经典、替代或凝集素途径。
所有这些途径都在 C3 激活水平上结合。形成的C3转化酶,将C3b分子沉积在细胞上,然后形成C5转化酶,激活末端补体蛋白 C5 至 C9 会生成膜插入复合物 C5b-7 、 C5b-8,最后生成 C5b-9,即“膜攻击复合物(MAC)”。所有这三种途径都会导致膜攻击复合物的形成和细胞裂解。
今天我们主要来说说“补体末端C5b-9复合物”在癌症中的作用。
裂解的C5b-9:抗肿瘤作用
支持补体激活的证据与抗肿瘤反应期间的 C5b-9 沉积有关,存在于多种人类恶性肿瘤中。补体系统的激活最终导致C5b-9末端补体复合物在细胞膜上组装,诱导靶细胞裂解。
在补体依赖性细胞毒性(CDC)期间成功实现细胞裂解需要在细胞表面形成多个C5b-9复合物。一旦C5b-8复合物暴露于C9,在细胞死亡之前会出现快速而广泛的 ATP 耗竭,腺嘌呤核苷酸 ATP、ADP 和 AMP 的泄漏。其他预溶性事件包括线粒体膜电位丧失,随之而来的 ATP 合成缺陷和剧烈的 Ca2+涌入,从而引发坏死性细胞死亡。
裂解性C5b-9对恶性信号通路的影响是多方面的,CDC已被证明使用几种坏死细胞死亡途径,涉及受体相互作用蛋白激酶1(RIPK1),受体相互作用蛋白激酶3(RIPK3)和混合谱系激酶结构域样蛋白(MLKL)。
肿瘤细胞通过C5b-9去除,膜补体调节蛋白(mCRPs)和其他细胞表面保护分子的表达以及可溶性补体抑制剂的分泌产生了“补体抗性”。细胞在初始补体介导的膜攻击中存活的能力使其能够抵抗未来的攻击。
使用基于mAb的免疫疗法刺激CDC对肿瘤细胞的破坏引起了很多兴趣。许多免疫疗法使用补体激活和 C5b-9 作为效应物来杀死肿瘤细胞。
这一系列事件表明:C5b-9在裂解环境中对肿瘤细胞是致命的,具有严格的“抗肿瘤”作用。
亚溶解水平C5b-9:促进肿瘤生长
近期的研究表明,当C5b-9被激活到“亚溶解”水平时,它反而通过几种机制“刺激肿瘤生长”。
组装在恶性细胞膜中亚溶解水平的C5b-9,产生几种不同的生物学反应:信号转导途径的激活,增殖和细胞凋亡的调节。
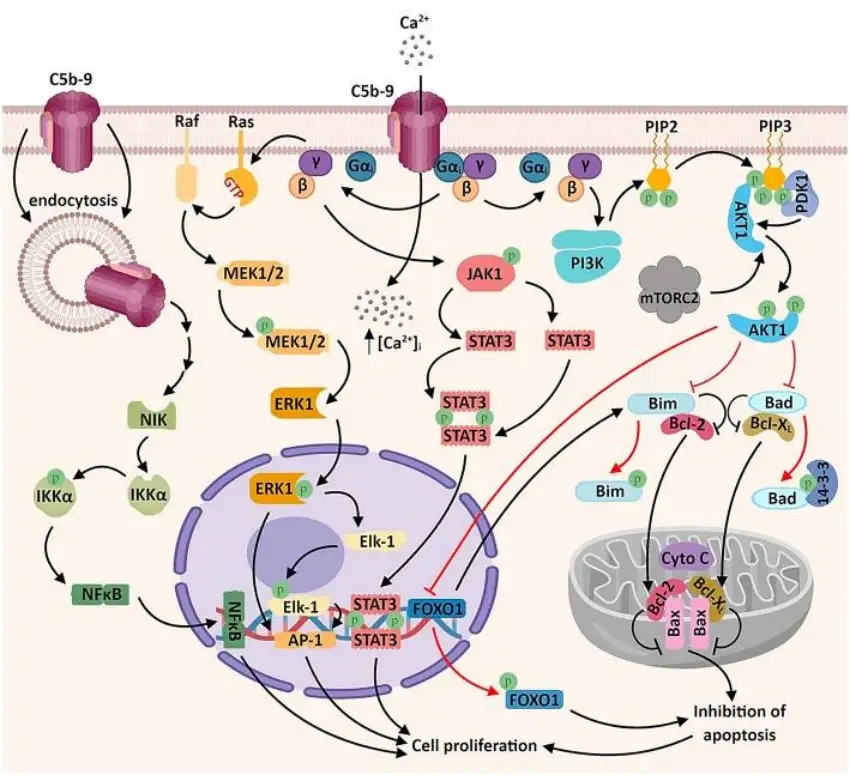
在调节癌症进展的信号转导网络中,已发现在亚溶解C5b-9下游起作用的是p38 / MAPK / JNK1和JAK1 / STAT3。
由亚溶解C5b-9诱导的细胞增殖依赖于Gi蛋白/ PI3K / Akt激酶和Ras / Raf-1 / ERK1途径的激活以及细胞周期特异性基因和原癌基因的调节。
亚溶解C5b-9诱导的NF-κB调节蛋白还可以进一步提高细胞存活率。
亚溶解 C5b-9 通过激活信号转导途径和调节癌症相关转录因子的活化来诱导细胞周期进程,同时保护肿瘤细胞免于凋亡。
此外,C5b-9还诱导补体反应基因RGC-32,该基因通过激活Akt和CDC2激酶有助于细胞周期调节。RGC-32 由肿瘤细胞表达并在癌症中发挥双重作用,通过支持恶性肿瘤的起始、进展、侵袭、转移和血管生成作为肿瘤启动子,或作为肿瘤抑制因子。
综合以上,C5b-9在癌症中的作用是无可争议的:通过治疗性地克服癌细胞中的CDC耐药性并增强C5b-9的抗肿瘤作用(从而增强基于mAb的免疫疗法的疗效),来抵消C5b-9的这些肿瘤促进性状,构成了免疫肿瘤学领域的下一个主要方向。
Biorbyt研发和生产的C5b-9兔多抗,在豚鼠 、大鼠等的多种组织中验证,助力免疫肿瘤学的研究。
产品信息:
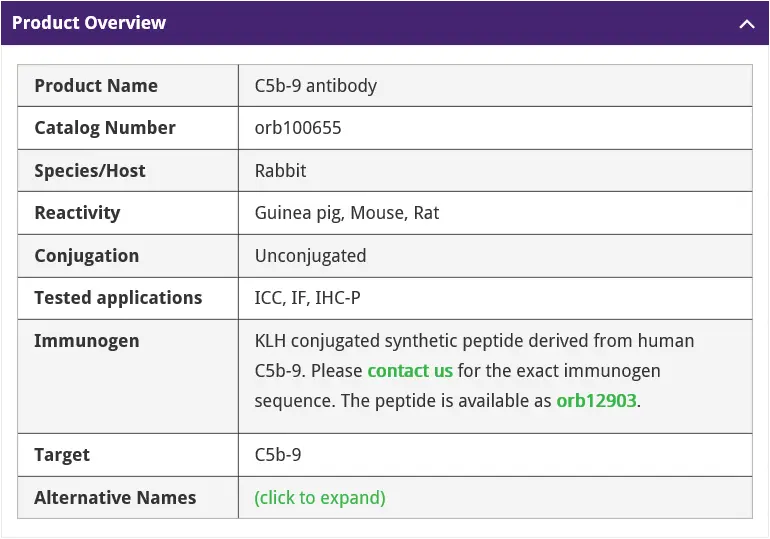
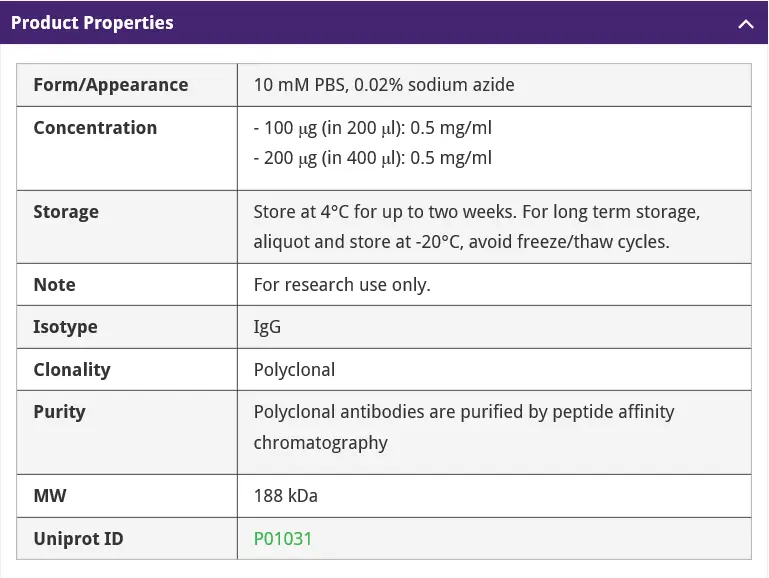
验证结果:
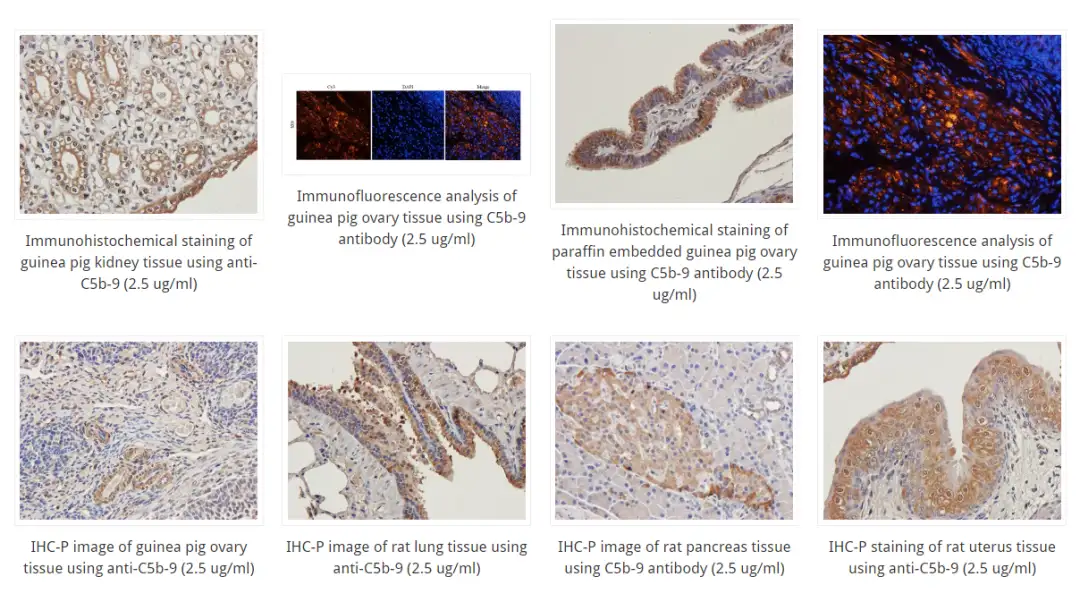
还有更多补体相关抗体产品,欢迎详询!
参考文献:
1.Vlaicu SI, Tatomir A, Rus V, Rus H. Role of C5b-9 and RGC-32 in Cancer. Front Immunol. 2019 May 9;10:1054. doi: 10.3389/fimmu.2019.01054.










