武汉博欧特生物科技有限公司
入驻年限:11 年
- 联系人:
王定涛
- 所在地区:
湖北 武汉市 洪山区
- 业务范围:
试剂、抗体、ELISA 试剂盒、技术服务、体外诊断
- 经营模式:
代理商
推荐产品
公司新闻/正文
IHC,WB 常见问题与结果解析
人阅读 发布时间:2023-08-28 08:48

免疫组化、Western都是免疫学三大工具之一。
免疫组化:融合了免疫学原理(抗原抗体特异性结合)和组织学技术(组织的取材、固定、包埋、切片、脱蜡、水化等),通过化学反应使标记抗体的显色剂 (荧光素、酶、金属离子、同位素)显色,来对组织(细胞)内抗原(多肽和蛋白质)进行定位、定性及相对定量的研究(主要是定位)。样本是细胞或组织,称为免疫组织化学技术(immunohistochemistry)或免疫细胞化学技术(immunocytochemistry)。要在显微镜下观察结果,可能出现膜阳性、质阳性和核阳性。
免疫印迹(immunoblotting)又称蛋白质印迹(Western blotting),是根据抗原抗体的特异性结合检测复杂样品中的某种蛋白的方法。先要进行SDS-PAGE,然后将分离开的蛋白质样品用电转仪转移到固相载体上,而后利用抗原-抗体-标记物显色来检测样品,可以用于定性和半定量。结合化学发光检测,可以同时比较多个样品同种蛋白的表达量差异。
免疫组化结果常见问题分析
1. 抗体浓度和质量问题以及抗体来源选择错误;
2. 抗原修复不全,换修复液或加强修复;
3. 组织切片本身这种抗原含量低,设阳性对照片;
4. 血清封闭时间过长;DAB 孵育时间过短;
6. 细胞通透不全,抗体未能充分进入胞内参与反应。
(二)非特异性染色的原因(着色一片黄/背景深)
1. 抗体孵育时间过长,抗体浓度;
2. 多抗易出现非特异性,可选择单抗;
3. 内源性过氧化物酶和生物素灭活不够;
4. 非特异性组分与抗体结合,延长血清封闭时间;
5. DAB 孵育时间过长或浓度过高;
6. PBS 冲洗不充分,残留抗体结果增强着色;
7. 标本染色过程中经常出现干片;
8. 脱蜡不充分;
9. 二抗与标本的内源性组织蛋白有交叉反应。
(三)染色弱阳性
1. 固定方式不当或固定时温度过高,影响到抗原的数量和质量;
2. 不适当的抗原修复方式,抗原决定簇暴露不足;
3. 抗体的稀释度是否过高或者孵育的温度/时间不足;
4. 孵育抗体前切片上遗留了过多的冲洗液;
5. 孵育时切片未放置水平,导致抗体孵育不均匀。
(四)信号定位与预测不符的原因
1. 组织固定不及时,抗原扩散移位;
2. 抗体选择错误;
3. 膜蛋白核质染色:抗原修复过长,导致细胞膜破坏,膜蛋白转移。
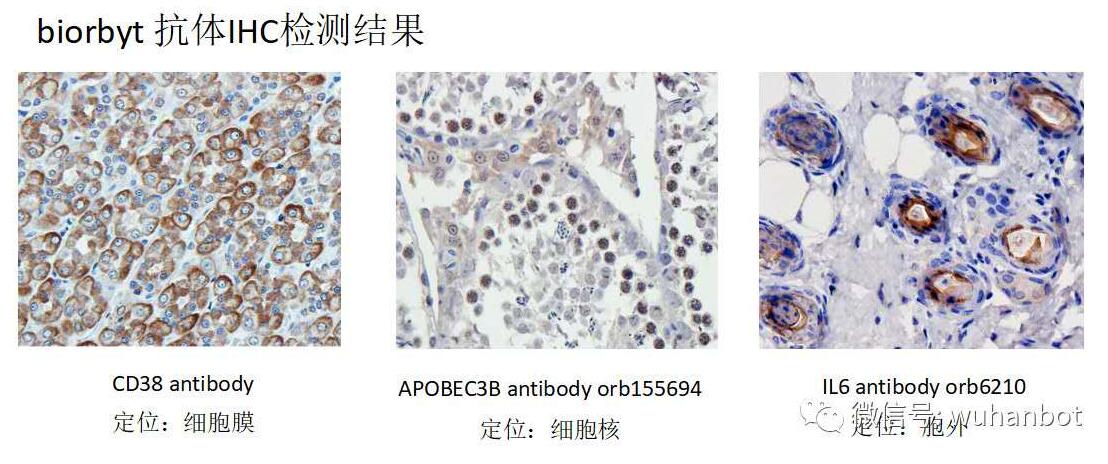
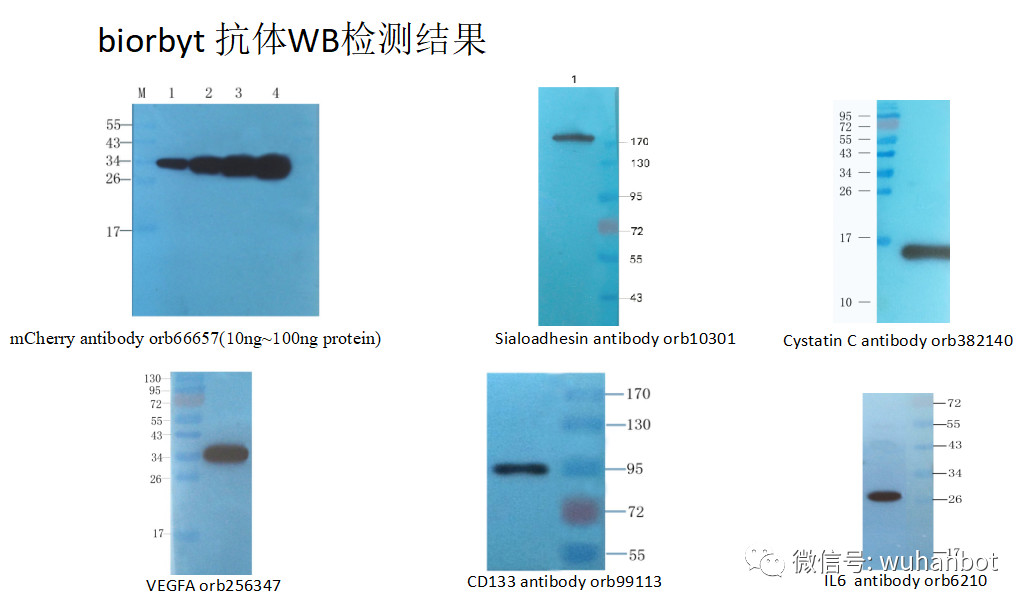
WB 结果常见问题分析
一. 高背景
1. 原因:封闭不好,一抗浓度高,洗膜时间和次数不够;
2. 优化:增加封闭时间,降低一抗浓度,增加洗膜时间和次数;
3. 解析:高背景是 WB 中最常见出现的问题,如果目的条带单一清晰,其他地方出现均一的背景,可以提高吐温比例,洗膜 5 min*5 次或者 10 min*3 次,不要图快肆意改时间和次数;如果出现非均一性背景,实验过程中要保持膜不被干;严格按照实验操作 SOP,养成好的实验习惯。
二. 空白片
1. 原因:比较多,最可能是一抗加错了,或者稀释时没取到亦或原管抗体没有混匀,再有可能二抗种属加错了,例如常见是兔的加成鼠的;转膜电压电流时间等;
2. 优化:仔细检查抗体是否加错,核实转膜设置没有问题;
3. 解析:胶片上一点信号都没有,多数情况是抗体加错了;如果中间出现了微弱的条带,可能原因是蛋白上样量太少,一抗浓度过低,ECL 发光液稀释过高或失效。若转膜出现了失误,比如膜放反了,肯定白片。
三. 非特异性条带
1. 原因:一抗有非特异性与蛋白结合;
2. 优化:更换一抗或参考「高背景」;
3. 解析:此种情况多数是因一抗不好,换一支抗体;设置好对照组区分目的条带;还有可能是一抗浓度过高引起的非特异性结合。
四. 条带有边缘规则的白圈
1. 原因:转膜时膜和胶之间存在气泡;
2. 优化:转膜前去掉膜和胶之间的气泡;
3. 解析:赶气泡太容易,省略。
五. 条带中间出现白斑点
1. 原因:底物消耗过快,中间区底物消耗完不发光了;
2. 优化:降低蛋白量,降低一抗和二抗的浓度;
3. 解析:快速操作,在中间部位底物消耗之前就把胶光片定影出来,一般实验员很难把控制;优先从降低蛋白量,降低一抗二抗浓度入手。
六. 出现黑点
1. 原因:膜上其他部位与一抗或者二抗非特异性结合;
2. 优化:封闭用的牛奶一定要纯并且完全溶解,封闭后至少洗膜一次;
3. 解析:确定封闭牛奶完全溶解,否则封闭时会导致不溶性颗粒附着在膜上,在发光时膜上会出现黑点;建议在牛奶溶解之后静止三分钟,轻取上层牛奶液进行封闭,封闭结束常规洗膜一次;孵育一抗或二抗时,需要加牛奶的也请参照此操作。
七. 条带拖尾
1. 原因:蛋白量太大,一抗浓度偏高和孵育时间太长;
2. 优化:根据实验需求调整上样蛋白量,调整一抗浓度和时间;
3. 解析:这种情况也是常见问题,上样蛋白量一般会做预实验避免;还有容易发生的是一抗浓度太高,作用时间太长引起的,品牌一抗都有稀释比例建议;再个质量好的一抗直接 37 度孵育半小时就好,无需孵育过夜;再强调一遍洗膜千万不要偷懒,次数和时间洗到位,不要担心把抗体和蛋白洗掉没那么脆弱。
八. 条带变形或奇型
1. 原因:配置胶有问题,胶中存在气泡或者某不溶性颗粒,电泳电流不均一;
2. 优化:配胶过程中要小心,使用无杂质的液体。
3. 解析:多数实验室使用设备都有些年限,比如配胶用的海绵垫或塑胶条等,用久了不密封出现漏液漏气;各 buffer 要注意不要有杂质;不使用边缘效应孔上样。
九. 其他问题
1. 条带连成一片。多数原因是上样量过多,其次是样品弥散或中途停止了电泳;
2. 条带偏高或者偏低。常有可能是蛋白有修饰现象;还有可能是胶的浓度与目的蛋白的浓度不对应,例如说 100KD 以上的蛋白用的 12% 胶跑,或者说 20KD 的蛋白用的 6% 胶跑;再是蛋白有降解,会在比原来位置低的地方出现主带,跟着出现一些其他条带,明显现象是所有的条带比正常的都低,且条带模糊不清晰。
欢迎访问biorbyt全球官方网站(www.biorbyt.com)和中国网站(www.biorbyt.com.cn),或者拨打biorbyt中国办事处热线电话:400-966-3101;027-87663101。 或微信(电话)15307197287在线沟通。










