武汉博欧特生物科技有限公司
入驻年限:11 年
- 联系人:
王定涛
- 所在地区:
湖北 武汉市 洪山区
- 业务范围:
试剂、抗体、ELISA 试剂盒、技术服务、体外诊断
- 经营模式:
代理商
推荐产品
公司新闻/正文
Biorbyt科研专题/ 癌症的标志 Hallmarks of Cancer
人阅读 发布时间:2021-03-05 15:55
Biorbyt科研专题/ 癌症的标志 Hallmarks of Cancer
原创 biorbyt 英国biorbyt收录于话题
#研究领域产品 28
#科研专题 1
#10周年活动 2
癌症背景
Cancer Background
尽管在我们对疾病的理解和治疗方面取得了许多新进展,但是癌症仍然是世界范围内主要的致死疾病之一。2018年全世界约有1810万新病例死亡,而其中950万例均与癌症相关。在美国,癌症仍是第二大主要死因。 据统计,在美国大约三分之一的人会在他们的生命周期中患上癌症。到2040年,预计每年新增癌症病例数将达到2950万,与癌症相关的死亡人数将达到1640万。 一般来说,在预期寿命、教育水平和生活水平较高的国家,如美国、加拿大和英国,癌症的发病率最高。然而,对于某些癌症类型,如宫颈癌则观察到相反的情况。 癌症原因和治疗 Cancer Causes and Treatments 癌症是由多种环境因素引起的,导致DNA损伤、遗传和子宫内突变。● 环境因素,如吸烟、过量的酒精摄入和辐射暴露,会提高个体患癌症的风险。● 遗传的基因突变诱导的癌症在所有癌症病例中约占5%-10%。● 特定基因中的50多个突变与遗传性癌症综合症有关。 癌症的标志性特征
Hallmarks of Cancer
癌症的典型特点包括在人类肿瘤的多步发展过程中获得的六种生理功能,这些功能建立在基因组不稳定性和炎症的基础上。在过去的十年中,对癌症的研究和日益加深的理解为建立核心能力提供了另外两个新的特点,即能量代谢的重新编程和逃避免疫破坏。肿瘤还表现出复杂性的另一个方面:除癌细胞外,肿瘤还包含大量募集在其表面上的正常细胞,这些细胞通过创建“肿瘤微环境”而有助于获得标志性特征。对这些概念的广泛适用性的认识日益影响着治疗人类癌症的新手段的发展。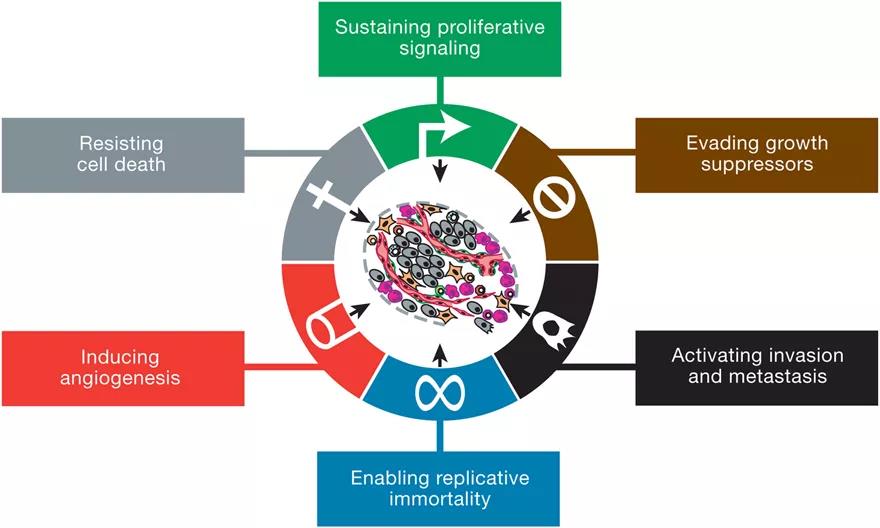
图1.癌症的标志。资料来源:Hanahan和Weinberg,2011年
1. 维持增殖信号 Sustaining Proliferative Signaling
癌细胞的基本特征是支持慢性增殖的能力。健康的组织会仔细调节细胞的生长和分裂周期,确保体内平衡以及标准的组织结构和功能。相反,癌细胞会破坏解除这些信号通路以维持其肿瘤的生长,与含有细胞内酪氨酸激酶结构域的细胞表面受体结合的生长因子(GF)受到主要影响。这将导致调节细胞周期进程和生长的细胞内信号通路的非正常上调。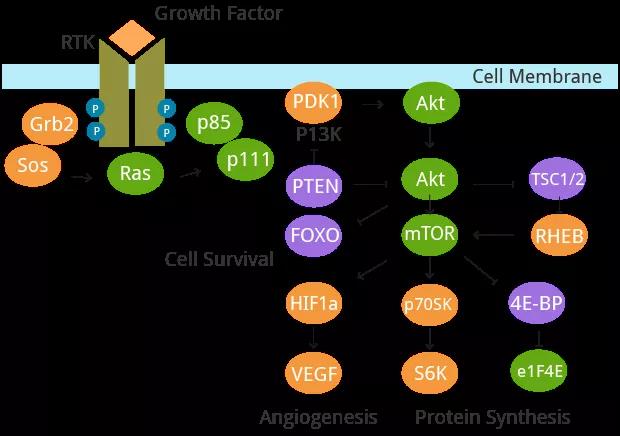
图2. 解除信号通路的调节
2. 逃避生长抑制物 Evading Growth Suppressors
许多肿瘤抑制物参与限制细胞生长和增殖。它们通常通过在癌细胞中的特征性失活而被发现。两种典型的肿瘤抑制因子是视网膜母细胞瘤相关的RB和TP53蛋白;它们是调控细胞凋亡、增殖和细胞衰老的重要调节因子。 尽管TP53和RB是细胞周期进程的重要调节剂,但它们也各自作为更广泛的机体网络的一部分运行,从而实现了功能冗余和自动备援。● 体内产生GF配体和同源受体,导致自分泌增殖刺激。● 癌细胞可以刺激周围基质中的正常细胞,为癌细胞提供各种生长因子。● 增加GF受体表达,使细胞反应增强。● 受体分子中的结构改变会增加配体非依赖性激活。● GF不依赖于信号通路的组成型下游激活,无需通过配体介导的受体激活刺激这些通路。● RB蛋白整合来自不同细胞外和细胞内来源的信号,作为细胞周期进程的关键看门分子,其缺失可导致持续的细胞增殖。● TP53受到细胞内应激源DNA损伤的输入,生长条件欠佳和体内稳态失衡会导致TP53停止细胞周期进程,直到条件良好为止;如果细胞损伤无法修复,则会启动细胞凋亡。● 活化的TP53的细微差别在很大程度上取决于环境,取决于细胞类型以及细胞应激和DNA损伤的严重程度。 有趣的是,RB(-)小鼠没有表现出增殖异常,观察到的唯。一肿瘤是生命后期的垂体瘤。[1] TP53(-)小鼠也表现出正常发育、正常的细胞和组织体内稳态,但在后期生命中又会发展为癌症,例如白血病和肉瘤。[2]
3. 激活侵袭和转移 Activating Invasion and Metastasis
一个特征明确的改变可以帮助癌细胞浸润和转移,从而帮助其浸润和转移。E-钙粘着蛋白(E-cadherin)通过与邻近的上皮细胞形成粘附连接来辅助上皮细胞片的组装并维持这些片内的细胞静止。E-钙粘蛋白在人类癌症中经常观察到下调和偶发突变失活,为其作为这种标志性功能的病毒抑制剂的作用提供了有力的支持。[3]癌转移的另一个重要驱动力是失去接触抑制作用。 接触抑制可确保健康的非癌细胞在相互接触时停止增殖和生长。当细胞进行恶性转化时,这种特性会丧失,从而导致不受控制的增殖和实体瘤的形成。[4]接触抑制可以通过多种方式实现:● 其中一种机制涉及一种肿瘤抑制蛋白Merlin(由NF2基因编码),当其缺失时会导致第二型遗传性神经纤维瘤病。Merlin通过将细胞表面粘附分子(例如,E-cadherin)偶联到跨膜受体酪氨酸激酶(例如,EGF受体)来调节接触抑制。这样,Merlin增强了钙粘蛋白介导的细胞间粘附。Merlin隔离生长因子受体,限制了癌细胞有效发射促有丝分裂信号的能力。 ●接触抑制的第二种机制需要LKB1上皮极性蛋白,该蛋白参与上皮结构组织和维持组织完整性。当LKB1在有组织的静态上皮结构中上调时,它已显示出可以抵消Myc癌基因的促有丝分裂作用。当LKB1表达减少时,上皮完整性受到损害,使上皮细胞更易受Myc诱导的转化。 在许多癌症中,其他粘附分子的表达显著改变,参与细胞停滞的那些表达下调。通常与胚胎发生和炎症期间的细胞运动相关的粘附分子主要上调。例如,N-cadherin在器官形成过程中通常表达于迁移神经元和间充质细胞,在许多侵袭性癌细胞中表达上调。[5]研究表明,在2D细胞培养中繁殖的健康细胞密集群体形成的细胞间接触寻求抑制进一步的细胞增殖,表现为融合的细胞单层。相反,在许多癌症类型中没有体外接触抑制,表明接触抑制是维持组织稳态的体外类似机制。
4. 实现复制永生 Enabling Replicative Immortality
癌细胞需要无限的复制潜能来形成肉眼可见的肿瘤,绕过在健康细胞中观察到的Hayflick限制,同时避免程序性细胞死亡。端粒和端粒酶在这一癌症特征中起关键作用。

染色体的端粒封端与癌细胞发展无限制增殖能力密切相关。 在培养物中繁殖的非永生化细胞中,端粒逐渐缩短,最终丧失了保护染色体末端免受端对端融合影响的能力。这些融合导致双着丝粒染色体的形成,从而扰乱细胞的核型,威胁生存能力。 端粒酶在非永生化细胞中主要不存在,但在绝大多数自生永生化细胞(如人癌细胞)中以显著的功能水平表达。 端粒酶活性的存在与对衰老和凋亡的抗性相关,癌细胞必须避免这种抗性以维持复制的永生。 研究表明,癌细胞由于无法表达显着的端粒酶水平,因此往往在多步肿瘤发展过程中相对较早地经历端粒丢失引起的危机。在恶变前的生长中观察到广泛侵蚀的端粒,以及端到端的染色体融合,表明癌细胞在获得端粒酶活性之前从健康细胞发育过程中已经经历了大量连续的端粒缩短细胞分裂。[6]
5. 诱导血管生成 Inducing Angiogenesis
癌细胞像健康细胞一样,需要营养和氧气,并具有清除代谢废物和二氧化碳以维持生存的能力。通过血管生成形成的与肿瘤相关的脉管系统满足了这些要求。在肿瘤发展和进展过程中,“血管生成开关”几乎总是被激活并保持开启状态,从而导致正常的静态脉管系统形成新的血管,从而有助于维持不断增长的肿瘤生长。[7]
图5.癌细胞血管生成
血管生成诱导和抑制最显著的原型是血管内皮生长因子- A (VEGF-A) 和血小板反应蛋白-1 (TSP-1)。

图6. VEGF信号通路
● 通过RTK的VEGFR-1–3产生的VEGF信号在多个水平上受到调节,说明其在血管发育和维持中的重要性。● 缺氧和通过致癌信号上调VEGF基因表达。● VEGF配体可以以潜伏形式螯合在细胞外基质中,这些潜伏形式可被细胞外基质降解蛋白酶如MMP-9释放和激活。● TSP-1结合内皮细胞显示的跨膜受体,抑制促血管生成刺激的活性。● 在肿瘤内产生的血管通常是异常的,表现为不规则的毛细血管发芽以及卷曲和过度的血管分支和扭曲。● 对癌前病变的组织学分析表明,在动物模型和人类侵袭性癌症的多阶段发展过程中,血管生成被意外地早期诱导。● 一旦血管生成被激活,肿瘤表现出不同类型的新生血管形成-胰腺导管腺癌是血管不足的,可能是主动抗血管生成的,而人肾和胰腺神经内分泌癌是血管密集的。 在过去的十年里,人们对血管生成的关注越来越多。在这丰富的新知识中,其他促血管生成信号,例如成纤维细胞生长因子 (FGF) 家族成员,在其表达显著上调时与维持肿瘤血管生成有关。然而,最近的研究表明,血管生成在肿瘤进展的癌前阶段也起着重要作用。
6. 阻止细胞正常死亡 Resisting Cell Death
众所周知,通过细胞凋亡程序化的细胞死亡是癌症发展的遗传防御机制。凋亡机制由上游调节剂和下游效应剂两部分组成。调节器分为两个主要通路:(1)外在程序涉及接收和处理细胞外死亡诱导信号;(2)内在程序负责感知和整合细胞内信号。 每个程序最终都激活一个主要是潜伏的蛋白酶(胱天蛋白酶8或9),该过程开始引发一连串的蛋白水解,涉及负责凋亡执行阶段的效应胱天蛋白酶,在此过程中,细胞逐渐被分解,然后被它的相邻的细胞和吞噬细胞消耗。目前,内在的凋亡程序被更广泛地认为是癌症发病机制的障碍。[9]
图7.细胞凋亡途径
细胞凋亡是细胞程序性死亡的过程,具有明显的形态学特征和能量依赖性生化机制。细胞凋亡被认为是包括正常细胞转换、免疫系统的适当发育和功能、激素依赖性萎缩、胚胎发育和化学诱导的细胞死亡在内的过程的重要组成部分。 凋亡细胞发生形态改变,包括广泛的质膜脱落和核破裂。凋亡小体是通过在一个叫做“萌芽”的过程中分离细胞碎片而形成的。它们由细胞质和紧密堆积的细胞器组成,有或没有核碎片。细胞器的完整性保持在完整的质膜内。这些小体随后被巨噬细胞、实质细胞或肿瘤细胞吞噬,并在吞噬溶酶体内降解。 在细胞凋亡中观察到三种主要的生化变化:半胱天冬酶的活化,DNA和蛋白质的分解,细胞膜的变化和吞噬细胞的识别。 癌细胞已经进化出多种策略来限制或规避细胞凋亡:● 最常见的机制涉及丧失TP53肿瘤抑制功能,从而从凋亡诱导电路中消除了关键的损伤传感器。● 癌细胞可能通过下调促凋亡因子(Bax,Bim,Puma)来增加抗凋亡调节因子的表达,例如Bcl-2,Bcl-xL或存活信号Igf1 / 2。● 或者,肿瘤也可以使外部配体诱导的死亡途径短路,从而避免细胞凋亡。 凋亡避免机制的多样性可能反映了肿瘤细胞人群在向恶性状态演变过程中所遇到的凋亡诱导信号的多样性。除了凋亡外,坏死还在抗细胞死亡中起作用;在某些情况下,坏死导致的细胞死亡似乎处于遗传控制之下,而不是一个随机和不协调的过程 坏死细胞死亡释放前炎症信号进入周围组织微环境,允许坏死细胞募集炎症细胞。证据表明,免疫炎性细胞可以在癌症背景下主动促进肿瘤生长,因为这些细胞可以促进血管生成、肿瘤细胞增殖和侵袭。此外,坏死细胞可释放生物活性调节因子,例如IL-1 α,其可直接刺激邻近活细胞增殖,具有促进癌症进展的潜力。[13]
结论 Conclusion
癌症的标志性特征包括在人类肿瘤多步发展过程中获得的六种生物学能力。这些特征构成了使癌症发展和进展的复杂性合理化的组织原则。从维持增殖信号转导到阻止细胞死亡,基因组不稳定会产生多种标志功能所需的遗传异常。在过去的十年中,癌症特征的概念上的进展呈现了另外两个特征:能量消化及代谢的重新编程和逃避免疫破坏。除了癌细胞外,肿瘤还表现出另一个复杂的方面:它们包含一个表面上正常的募集细胞库,这些细胞通过创造“肿瘤微环境”来促进标志性特征的获得。认识到这些概念的广泛适用性将日益影响治疗人类癌症的新方法的发展。
参考文献
1. Lipinski MM, Jacks T. The retinoblastoma gene family in differentiation and development. Oncogene. 1999 Dec 20;18(55):7873-82. doi: 10.1038/sj.onc.1203244. PMID: 10630640.
2. Ghebranious N, Donehower LA. Mouse models in tumor suppression. Oncogene. 1998 Dec 24;17(25):3385-400. doi: 10.1038/sj.onc.1202573. PMID: 9917000.
3. Berx G, van Roy F. Involvement of members of the cadherin superfamily in cancer. Cold Spring Harb Perspect Biol. 2009 Dec;1(6):a003129. doi: 10.1101/cshperspect.a003129. Epub 2009 Sep 23. PMID: 20457567; PMCID: PMC2882122.
4. Pavel, M., Renna, M., Park, S.J. et al. Contact inhibition controls cell survival and proliferation via YAP/TAZ-autophagy axis. Nat Commun 9, 2961 (2018). https://doi.org/10.1038/s41467-018-05388-x
5. Cavallaro U, Christofori G. Cell adhesion and signalling by cadherins and Ig-CAMs in cancer. Nat Rev Cancer. 2004 Feb;4(2):118-32. doi: 10.1038/nrc1276. PMID: 14964308.
6. Cleal K, Norris K, Baird D. Telomere Length Dynamics and the Evolution of Cancer Genome Architecture. Int J Mol Sci. 2018;19(2):482. Published 2018 Feb 6. doi:10.3390/ijms19020482.
7. Hanahan D, Folkman J. Patterns and emerging mechanisms of the angiogenic switch during tumorigenesis. Cell. 1996 Aug 9;86(3):353-64. doi: 10.1016/s0092-8674(00)80108-7. PMID: 8756718.
8. Baeriswyl V, Christofori G. The angiogenic switch in carcinogenesis. Semin Cancer Biol. 2009 Oct;19(5):329-37. doi: 10.1016/j.semcancer.2009.05.003. Epub 2009 May 29. PMID: 19482086.
9. Adams JM, Cory S. The Bcl-2 apoptotic switch in cancer development and therapy. Oncogene. 2007 Feb 26;26(9):1324-37. doi: 10.1038/sj.onc.1210220. PMID: 17322918; PMCID: PMC2930981.
10. Adams JM, Cory S. The Bcl-2 apoptotic switch in cancer development and therapy. Oncogene. 2007 Feb 26;26(9):1324-37. doi: 10.1038/sj.onc.1210220. PMID: 17322918; PMCID: PMC2930981.
11. Galluzzi L, Kroemer G. Necroptosis: a specialized pathway of programmed necrosis. Cell. 2008 Dec 26;135(7):1161-3. doi: 10.1016/j.cell.2008.12.004. PMID: 19109884.
12. Zong WX, Thompson CB. Necrotic death as a cell fate. Genes Dev. 2006 Jan 1;20(1):1-15. doi: 10.1101/gad.1376506. PMID: 16391229.
13. Grivennikov SI, Greten FR, Karin M. Immunity, inflammation, and cancer. Cell. 2010 Mar 19;140(6):883-99. doi: 10.1016/j.cell.2010.01.025. PMID: 20303878; PMCID: PMC2866629.
资料来源
● International Agency for Research on Cancer- https://www.iarc.who.int/
● Cancer Research UK- https://www.cancerresearchuk.org/
● Hallmarks of Cancer- Hanahan D, Weinberg RA. Hallmarks of cancer: the next generation. Cell. 2011 Mar 4;144(5):646-74. doi: 10.1016/j.cell.2011.02.013. PMID: 21376230.
● Innovative Approaches for Cancer Treatment- Pucci C, Martinelli C, Ciofani G. Innovative approaches for cancer treatment: current perspectives and new challenges. Ecancermedicalscience. 2019;13:961. doi: 10.3332/ecancer.2019.961. PMID: 31537986; PMCID: PMC6753017.
biorbyt拥有各种研究领域的抗体,蛋白和试剂盒,欢迎访问biorbyt全球官方网站(www.biorbyt.com)和中国网站(www.biorbyt.com.cn),或者拨打biorbyt中国办事处热线电话:400-966-3101;027-87663101。 或微信(电话)15307197287在线沟通。










